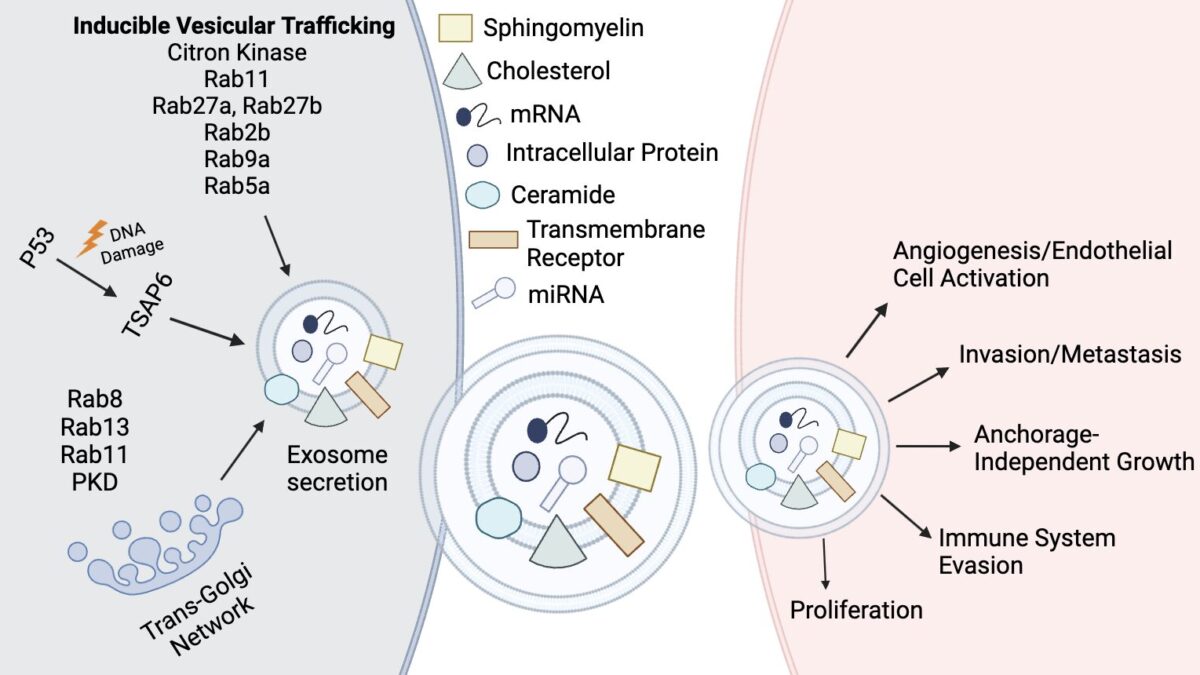
Exosome và sự tiến triển của ung thư
25/02/2025
Phương pháp xử lý dữ liệu Proteomics
03/03/2025TỔNG QUAN VỀ PHOSPHOLIPID
Phospholipid là một loại chất béo đặc biệt có một đầu ưa nước (phân cực) và một đầu kỵ nước (không phân cực), đây là đặc điểm quan trọng tạo nên cấu trúc và chức năng của màng tế bào. Đóng vai trò then chốt trong nhiều quá trình sinh học quan trọng của tế bào, bao gồm duy trì tính thấm chọn lọc của màng, tham gia vào quá trình truyền tín hiệu nội bào và vận chuyển lipid. Nhờ vào đặc tính sinh học đa dạng, phospholipid được ứng dụng rộng rãi trong công nghệ dược phẩm, công nghiệp thực phẩm và mỹ phẩm.
Dựa trên cấu trúc, phospholipid được phân thành hai nhóm chính là glycerophospholipid và sphingophospholipid, cùng với các phân nhóm đặc biệt như lysophospholipid và cardiolipin, mỗi loại có tính chất hóa sinh và chức năng đặc trưng.
Glycerophospholipid
Glycerophospholipid là nhóm phospholipid có cấu trúc gồm bộ khung glycerol, hai chuỗi acid béo, và một nhóm đầu chứa phosphate, đóng vai trò quan trọng trong sự linh động của màng tế bào và các quá trình truyền tín hiệu nội bào.
Một số phân nhóm quan trọng bao gồm:
- Phosphatidylcholine (PC): Loại glycerophospholipid phổ biến nhất trong màng tế bào nhân thực, có vai trò thiết yếu trong cấu trúc màng và chức năng của lipoprotein.
- Phosphatidylethanolamine (PE): Xuất hiện chủ yếu trong màng ty thể và màng nội bào, hỗ trợ tính linh hoạt của màng và quá trình từ thực bào (autophagy).
- Phosphatidylserine (PS): Tham gia vào quá trình apoptosis (chết tế bào theo chu trình) và đông máu, đồng thời đóng vai trò quan trọng trong chức năng thần kinh.
- Phosphatidylinositol (PI): Là tiền chất của phosphoinositide, giúp điều hòa tín hiệu tế bào, tăng trưởng và vận chuyển qua màng.
- Phosphatidylglycerol (PG): chất hoạt động trên bề mặt của phổi, đồng thời là tiền chất của cardiolipin, hỗ trợ sự ổn định của màng ty thể.
Sphingophospholipid
Khác với glycerophospholipid, sphingophospholipid có bộ khung sphingosine thay vì glycerol. Đại diện của nhóm này là sphingomyelin, một thành phần chính của lớp myelin bao quanh dây thần kinh, giúp bảo vệ tế bào thần kinh và hỗ trợ truyền tín hiệu tế bào.
Lysophospholipid
Lysophospholipid được hình thành thông qua quá trình thủy phân enzyme, hoạt động như phân tử tín hiệu sinh học, có liên quan đến viêm nhiễm và các phản ứng sinh lý của tế bào.
Bao gồm một số loại lysophospholipid phổ biến:
- Lysophosphatidylcholine (LPC): Góp phần vào phản ứng viêm và sự hình thành xơ vữa động mạch.
- Lysophosphatidic acid (LPA): Điều hòa tăng sinh tế bào, di chuyển và quá trình di căn ung thư.
Cardiolipin
Cardiolipin là một glycerophospholipid đặc trưng của màng trong ty thể, có vai trò thiết yếu trong duy trì tính toàn vẹn của chuỗi hô hấp và điều hòa phosphoryl hóa oxy hóa. Thông qua tương tác với các phức hợp hô hấp, đặc biệt là cytochrome C oxidase, cardiolipin ổn định tổ chức màng, tối ưu hóa truyền electron và tổng hợp ATP. Sự oxy hóa hoặc tái cấu trúc cardiolipin làm suy giảm chức năng ty thể và kích hoạt apoptosis.
Một số phương pháp chiết xuất phospholipid
Bảng 1. Một số phương pháp chiết xuất phospholipid (Kieu Giang Le, Research Intern, Hoan Vu Biomolecules., JSC)
| Phương pháp | Quy trình |
| Chiết xuất bằng dung môi | 1. Cân mẫu (~1-5 g), nghiền nhỏ. |
| Chiết xuất bằng chất lỏng siêu tới hạn (SFE) | 1. Chuẩn bị mẫu khô/đông lạnh, nghiền nhỏ. |
| Chiết xuất bằng enzyme | 1. Hòa mẫu vào dung dịch đệm (pH 7.4–8.0). |
| Chiết xuất từ vi sinh vật và vi tảo | 1. Nuôi cấy vi sinh vật hoặc vi tảo trong điều kiện tối ưu. |
Bảng 2. So sánh các chiết xuất phospholipid (Kieu Giang Le, Research Intern, Hoan Vu Biomolecules., JSC)
| Tiêu chí | Chiết xuất bằng dung môi | Chiết xuất bằng chất lỏng siêu tới hạn (SFE) | Chiết xuất bằng enzyme | Chiết xuất từ vi sinh vật và vi tảo |
|---|---|---|---|---|
| Phương pháp | Dùng dung môi hữu cơ hòa tan và tách lipid. | Dùng CO₂ siêu tới hạn để hòa tan lipid. | Dùng enzyme phân hủy liên kết ester của phospholipid. | Phá vỡ tế bào vi sinh vật/vi tảo để giải phóng lipid. |
| Hiệu suất chiết xuất | Cao, nhưng có thể chiết cả lipid không mong muốn. | Trung bình đến cao, tùy áp suất và nhiệt độ. | Cao với phospholipid có liên kết ester dễ bị thủy phân. | Thấp hơn phương pháp hóa học nhưng có thể cải thiện. |
| Tính chọn lọc | Không cao, có thể chiết nhiều loại lipid khác nhau. | Có thể tối ưu hóa để chọn lọc lipid mong muốn. | Chọn lọc cao, nhắm vào phospholipid cụ thể. | Phụ thuộc vào phương pháp phá vỡ tế bào. |
| An toàn & Môi trường | Dung môi hữu cơ độc hại, có thể gây ô nhiễm. | Không dùng dung môi độc hại, thân thiện môi trường. | Không độc hại, thân thiện với môi trường. | Sử dụng nguồn tái tạo, ít gây ô nhiễm. |
| Ứng dụng | Phân tích lipid, sản xuất thực phẩm, dược phẩm. | Dược phẩm, thực phẩm chức năng, nghiên cứu lipid. | Thực phẩm, y sinh học, nghiên cứu enzyme. | Sản xuất bio-lipid, nghiên cứu năng lượng sinh học. |
| Nhược điểm | Sử dụng dung môi độc hại, cần xử lý an toàn. | Cần thiết bị chuyên dụng, chi phí cao. | Enzyme đắt, thời gian xử lý lâu. | Hiệu suất thấp, yêu cầu tinh chế phức tạp. |
| Ưu điểm | Đơn giản, hiệu quả cao. | Không cần dung môi độc hại, bảo toàn cấu trúc lipid. | Chọn lọc lipid tốt, thân thiện với môi trường. | Sử dụng nguồn nguyên liệu bền vững, ít tác động môi trường. |
Phân tích phospholipid bằng khối phổ
Sau khi chiết xuất phospholipid, phương pháp sắc ký – khối phổ được sử dụng để xác định thành phần, cấu trúc và đặc điểm của các hợp chất trong mẫu.
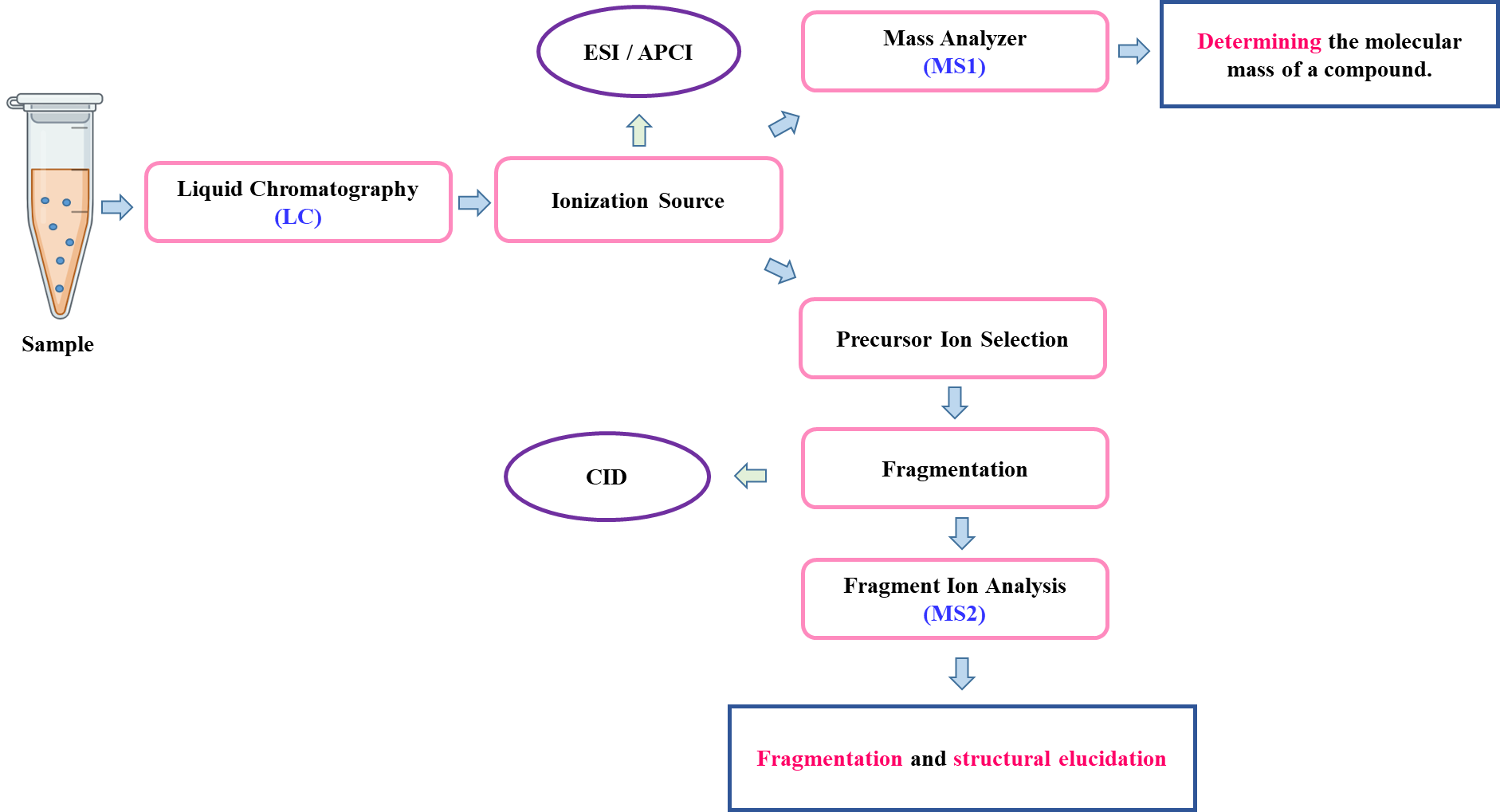
Hình 1. Sơ đồ tổng quát của phương pháp sắc ký-khối phổ (Kieu Giang Le, Research Intern, Hoan Vu Biomolecules., JSC)
LC-MS (Liquid Chromatography – Mass Spectrometry) và LC-MS/MS (Liquid Chromatography – Tandem Mass Spectrometry) là các kỹ thuật phân tích hiện đại, kết hợp giữa sắc ký lỏng hiệu năng cao (HPLC/UPLC) và khối phổ (MS) để xác định chính xác khối lượng phân tử( m/z), thành phần và cấu trúc hóa học của các hợp chất trong một mẫu phức tạp.
Trong LC-MS, mẫu sẽ được phân tách bằng sắc ký lỏng dựa trên tương tác giữa pha động và pha tĩnh, sau đó đi vào nguồn ion hóa (ESI, APCI), nơi các phân tử được chuyển thành ion. Các ion này được dẫn vào bộ phân tích khối phổ (MS1) để đo tỷ lệ m/z của ion tiền chất, cung cấp thông tin về khối lượng phân tử của hợp chất.
LC-MS/MS mở rộng khả năng phân tích thông qua khối phổ hai lần (MS/MS), cho phép xác định đặc trưng cấu trúc của hợp chất thông qua quá trình phân mảnh ion có kiểm soát (CID – Collision-Induced Dissociation). Sau khi ion tiền chất được lựa chọn trong MS1, nó đi vào buồng va chạm, nơi xảy ra sự phân mảnh có chủ đích để tạo thành các ion phân mảnh đặc trưng. Các ion phân mảnh này tiếp tục được phân tích trong MS2, cung cấp thông tin chi tiết về đặc điểm cấu trúc và thành phần phân tử của hợp chất.
Với độ nhạy và độ chọn lọc cao, LC-MS và LC-MS/MS đóng vai trò quan trọng trong phân tích dược phẩm, hóa sinh, môi trường và pháp y, cho phép định lượng chính xác và định danh hợp chất ở nồng độ vết trong các hệ nền phức tạp.
Bảng 3. So sánh MS1 và MS2 trong LC-MS/MS (Kieu Giang Le, Research Intern, Hoan Vu Biomolecules., JSC)
| Tiêu chí | MS1 (Khối phổ lần 1) | MS2 (Khối phổ lần 2) |
|---|---|---|
| Chức năng chính | Xác định khối lượng phân tử của ion tiền chất (precursor ion). | Phân mảnh ion tiền chất để xác định đặc trưng cấu trúc phân tử (product ions). |
| Cơ chế hoạt động | Đo phổ khối của tất cả các ion sinh ra từ nguồn ion hóa mà không có quá trình phân mảnh. | Chọn một ion tiền chất cụ thể, sau đó kích thích phân mảnh trong buồng va chạm để tạo ra các ion phân mảnh. |
| Phương pháp phân mảnh | Không có quá trình phân mảnh. | Sử dụng kỹ thuật phân mảnh như CID (Collision-Induced Dissociation), HCD (Higher-energy Collisional Dissociation), hoặc ETD (Electron Transfer Dissociation) để tạo ra phổ khối của các ion phân mảnh. |
| Dữ liệu đầu ra | Danh sách các ion với tỷ lệ khối lượng trên điện tích (m/z), đại diện cho các phân tử chưa bị phân mảnh. | Phổ khối của các ion phân mảnh, cung cấp thông tin về mô hình phân mảnh và đặc trưng cấu trúc phân tử. |
| Độ chọn lọc | Thấp hơn, do không có quá trình phân mảnh nên có thể có sự chồng chéo của các tín hiệu từ nhiều hợp chất khác nhau. | Cao hơn, do quá trình chọn lọc ion tiền chất và phân mảnh giúp xác định chính xác hợp chất đích. |
| Ứng dụng | Phù hợp cho phân tích sơ bộ, sàng lọc hợp chất dựa trên khối lượng phân tử. | Phù hợp cho phân tích chuyên sâu, xác định cấu trúc và định danh chính xác hợp chất. |
| Khả năng định danh | Xác định khối lượng phân tử nhưng không cung cấp thông tin chi tiết về cấu trúc phân tử. | Cho phép xác định cấu trúc phân tử nhờ vào mô hình phân mảnh đặc trưng. |
| Tính đặc hiệu | Thấp hơn, có thể xảy ra nhiễu do các hợp chất có khối lượng phân tử tương tự. | Cao hơn, do mô hình phân mảnh đặc trưng của mỗi hợp chất. |
| Ứng dụng điển hình | Sàng lọc hợp chất, xác định sơ bộ các chất có trong mẫu. | Định danh chính xác hợp chất, xác định đồng phân, phân tích đặc trưng cấu trúc của peptide, lipid, hoặc các hợp chất hữu cơ phức tạp. |
Hệ thống sắc ký-khối phổ trong lipidomics và bệnh lý
Các nghiên cứu gần đây đã làm sáng tỏ vai trò quan trọng của hệ thống sắc ký-khối phổ trong lipidomics, đặc biệt trong phân tích lipid liên quan đến các bệnh lý như tiểu đường, viêm mãn tính, rối loạn thần kinh và tim mạch. Những nghiên cứu này không chỉ đánh giá các phương pháp sắc ký và khối phổ hiện đại mà còn xem xét toàn bộ quy trình phân tích lipid, từ xử lý mẫu đến diễn giải dữ liệu. Đặc biệt, LC-MS và LC-MS/MS được nhấn mạnh là công cụ thiết yếu giúp xác định chính xác và phân loại đa dạng các loại lipid trong hệ sinh học.
Trong lĩnh vực miễn dịch học, một nghiên cứu khác đã sử dụng sắc ký lỏng kết hợp với khối phổ (HILIC-MS/MS) để phân tích lipid trong tế bào bạch cầu đơn nhân từ máu ngoại vi (PBMCs). Kết quả giúp xác định hơn 200 loại lipid khác nhau, cung cấp thông tin chi tiết về vai trò của glycerophospholipid và sphingolipid trong hệ miễn dịch.
Ngoài ra, hệ thống sắc ký-khối phổ cũng được ứng dụng trong nghiên cứu các bệnh thoái hóa thần kinh, giúp xác định các chỉ dấu sinh học lipid tiềm năng và hướng đến các mục tiêu điều trị mới.
Tài liệu tham khảo
Phospholipid Extraction Methods
Folch, J., Lees, M., & Sloane Stanley, G. H. (1957). A simple method for the isolation and purification of total lipides from animal tissues. Journal of Biological Chemistry, 226(1), 497–509. https://doi.org/10.1016/S0021-9258(18)64849-5
Bligh, E. G., & Dyer, W. J. (1959). A rapid method of total lipid extraction and purification. Canadian Journal of Biochemistry and Physiology, 37(8), 911–917. https://doi.org/10.1139/o59-099
Kuksis, A. (2000). Lipid extraction, fractionation, and analysis. Trong R. J. Hamilton & J. Cast (Biên tập), Lipid Analysis (tr. 1–45). Oxford University Press.
Mass Spectrometry Analysis of Phospholipids
Han, X., & Gross, R. W. (2005). Shotgun lipidomics: Electrospray ionization mass spectrometric analysis and quantitation of cellular lipidomes directly from crude extracts of biological samples. Mass Spectrometry Reviews, 24(3), 367–412. https://doi.org/10.1002/mas.20023
Murphy, R. C. (2014). Tandem mass spectrometry of lipids: Molecular analysis of complex lipids. Royal Society of Chemistry.
Pulfer, M., & Murphy, R. C. (2003). Electrospray mass spectrometry of phospholipids. Mass Spectrometry Reviews, 22(5), 332–364. https://doi.org/10.1002/mas.10061
Phospholipid Extraction from Microorganisms and Microalgae
Ryckebosch, E., Bruneel, C., Termote-Verhalle, R., Goiris, K., Muylaert, K., & Foubert, I. (2014). Influence of extraction solvent system on extractability of lipid components from different microalgae species. Algal Research, 3, 36–43. https://doi.org/10.1016/j.algal.2013.11.001
Halim, R., Danquah, M. K., & Webley, P. A. (2012). Extraction of oil from microalgae for biodiesel production: A review. Biotechnology Advances, 30(3), 709–732. https://doi.org/10.1016/j.biotechadv.2012.01.001
Research Applications in Lipidomics
Cajka, T., & Fiehn, O. (2016). Toward Merging Untargeted and Targeted Methods in Mass Spectrometry-Based Metabolomics and Lipidomics. Analytical Chemistry, 88(1), 524–545. https://doi.org/10.1021/acs.analchem.5b04491
Sandra, K., dos Santos Pereira, A., Vanhoenacker, G., David, F., & Sandra, P. (2010). Comprehensive blood plasma lipidomics by liquid chromatography/quadrupole time-of-flight mass spectrometry. Journal of Chromatography A, 1217(25), 4087–4099. https://doi.org/10.1016/j.chroma.2010.02.034
Ventura, G., Bianco, M., Calvano, C. D., Losito, I., & Cataldi, T. R. I. (2024). Tandem Mass Spectrometry in Untargeted Lipidomics: A Case Study of Peripheral Blood Mononuclear Cells. International Journal of Molecular Sciences, 25(22), 12077. https://doi.org/10.3390/ijms252212077【7】.
Han, X., & Gross, R. W. (2005). Shotgun lipidomics: Electrospray ionization mass spectrometric analysis and quantitation of cellular lipidomes directly from crude extracts of biological samples. Mass Spectrometry Reviews, 24(3), 367–412. https://doi.org/10.1002/mas.20023