Liquid chromatography-high resolution mass spectrometry for the analysis of bioactive natural products
24/02/2025
TỔNG QUAN VỀ PHOSPHOLIPID
27/02/2025Exosome và sự tiến triển của ung thư
Uyen Nguyen (Research Officer, Hoan Vu Biomolecules., JSC.)
Exosome
Exosome là các túi ngoại bào có màng bao bọc (EV) có đường kính từ 40 nm đến 160 nm có nguồn gốc từ khoang nội thể. Exosome chứa nhiều hàng hóa có hoạt tính sinh học, bao gồm axit nucleic (DNA, mRNA, microRNA, RNA dài không mã hóa), protein, lipid và chất chuyển hóa. Chúng hoạt động như các chất truyền tin trong tế bào và có chức năng thay đổi hoạt động sinh học của các tế bào nhận. Chúng trải qua quá trình nảy chồi và hình thành nhiều túi (MVB), và hợp nhất với màng tế bào (PM), và cuối cùng được giải phóng ra bên ngoài tế bào. Ngoài ra, exosome cũng có thể được nội bào hóa bằng nội bào bên trong tế bào và vật chất của nó được đưa đến tế bào đích, do đó thay đổi chức năng sinh học của tế bào.
Exosome và ung thư
Gần đây, các tác động bệnh sinh lý của exosome đối với các bệnh, đặc biệt là ung thư, đã xuất hiện. Bản chất và số lượng của hàng hóa EV1 là đặc hiệu cho từng loại tế bào và liên quan đến một số trạng thái sinh lý và tình trạng bệnh lý, bao gồm quá trình hình thành khối u, tình trạng viêm, đông máu và các tình trạng khác2. Exosome có nguồn gốc từ khối u được báo cáo là có liên quan đến sự phát triển của bệnh ác tính ung thư bằng cách thúc đẩy sự phát triển của ung thư, thiết lập một hốc tiền di căn và điều chỉnh khả năng kháng thuốc3, 4. So với tế bào bình thường, tế bào ung thư sản xuất và tiết ra nhiều protein, axit nucleic và lipid hơn. Các chất này cần dựa vào exosome làm chất mang để vận chuyển giữa các tế bào, dẫn đến tạo ra một số lượng lớn exosome liên quan đến khối u. Đường kính của exosome của khối u thường là 30-100 nm và exosome khối u là chất trung gian quan trọng của vi môi trường khối u. Chúng đóng vai trò quan trọng trong sự xuất hiện và phát triển của ung thư. Nó hướng dẫn sự tương tác giữa các loại tế bào khác nhau trong vi môi trường khối u. Do đó, nó là một sứ giả truyền tín hiệu liên lạc giữa các tế bào quan trọng trong quá trình di căn và xâm lấn của tế bào ung thư.

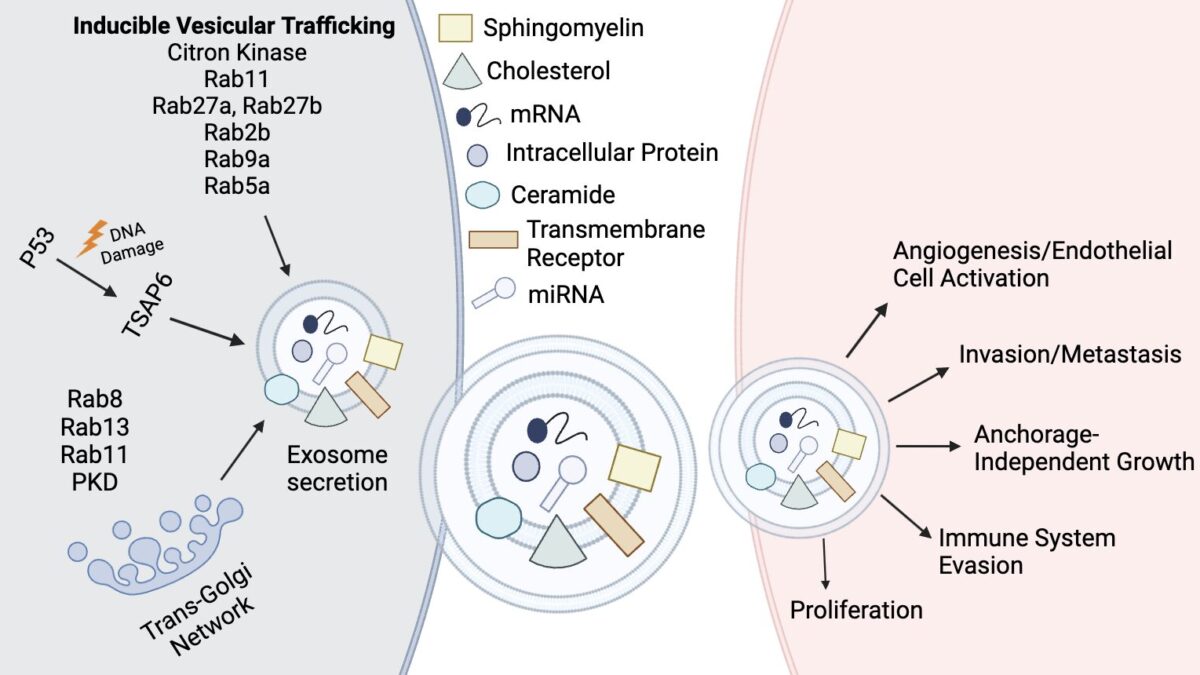
Hình 1 – Sơ đồ tiết exosome trong mô hình tế bào ung thư ((Uyen Nguyen, Research Officer, Hoan Vu Biomolecules., JSC.)
Exosome đóng vai trò thúc đẩy sự tăng sinh khối u và thay đổi môi trường vi mô trong môi trường vi mô khối u trong quá trình phát triển khối u. Exosome liên quan đến khối u trong quá trình thúc đẩy sự tăng sinh khối u, các chất đại phân tử sinh học có trong exosome được bảo vệ bởi lớp kép lipid. Vì lý do này, chúng có thể được bảo vệ khỏi quá trình thủy phân bằng enzym hoặc các chất khác. Sau khi exosome khối u liên kết với thụ thể, nó có thể thay đổi chức năng và kiểu hình của các tế bào thụ thể, từ đó ảnh hưởng đến các tế bào không phải khối u và tạo ra môi trường vi mô khối u thuận lợi cho các tế bào khối u.
Ngoài việc thúc đẩy sự tăng sinh tế bào khối u, exosome liên quan đến khối u có thể thay đổi môi trường vi mô khối u, chủ yếu ở chỗ chúng có thể gây ra sự hình thành các mạch máu, cung cấp chất dinh dưỡng và loại bỏ chất thải cho sự phát triển của các tế bào khối u và thúc đẩy sự chuyển giao và xâm lấn của ung thư. Exosome có thể chuyển các đại phân tử axit nucleic quan trọng trong tế bào khối u sang các tế bào bình thường theo dòng máu, do đó gây ra khả năng xâm lấn của chúng. Đồng thời, khi các exosome có nguồn gốc được thụ thể tiếp nhận, chúng có thể thay đổi kiểu hình của thụ thể, do đó tạo ra một hốc tiền di căn tốt cho sự xâm lấn và di căn của tế bào khối u và hoàn thành quá trình xâm lấn, và sau khi xâm nhập vào mạch máu, exosome có thể điều chỉnh môi trường bên ngoài của tế bào khối u và thúc đẩy tế bào khối u đến đích xâm chiếm.
Chiến lược điều trị ung thư dựa trên exosome
EV có thể được tìm thấy trong hầu hết các loại dịch cơ thể; sau khi EV được phân lập từ các mẫu sinh học (ví dụ: huyết tương hoặc nước tiểu), protein hoặc các phân tử sinh học khác trong EV có thể được xác định và định lượng bằng các chiến lược omics tiên tiến, bao gồm cả phép đo axit nucleic và protein. Mặc dù đã có nhiều nghiên cứu về hàng hóa RNA trong exosome, việc kiểm tra thành phần protein của exosome cung cấp những hiểu biết mới về cả chức năng và vị trí tế bào gốc của exosome, đặc biệt là khi các sửa đổi sau dịch mã (PTM) được đưa vào phân tích.
Exosome có thể được sử dụng làm chất trung gian cho các can thiệp điều trị ung thư, chủ yếu phản ánh việc giải phóng các exosome có nguồn gốc từ khối u để kiểm soát sự tiến triển của ung thư, và cấu trúc phân tử tự nhiên và chức năng sinh học đặc biệt của exosome có thể được sử dụng làm chất vận chuyển thuốc tự nhiên. Trong quá trình ức chế việc giải phóng các exosome có nguồn gốc từ khối u, người ta thấy rằng việc nhắm mục tiêu vào protein Rab có thể ức chế hiệu quả việc giải phóng các exosome. Về mặt sử dụng exosome làm chất vận chuyển tự nhiên để điều trị ung thư, cấu trúc tự nhiên của exosome như protein màng và lipid độc đáo của nó có thể hỗ trợ exosome liên kết với các thụ thể cụ thể, do đó cải thiện hiệu quả phân phối thuốc. Các nghiên cứu đã chỉ ra rằng phương pháp điện di doxorubicin (Dox) vào exosome và ứng dụng vào dòng tế bào ung thư vú có thể giúp các exosome được thiết kế có thể đưa Dox đến mô khối u một cách cụ thể, qua đó ức chế sự phát triển của khối u và cuối cùng đạt được mục tiêu điều trị ung thư.
Phân tích proteomics dựa trên khối phổ nâng cao (MS) đã nổi lên như một công cụ mạnh mẽ để lập hồ sơ proteome toàn cầu định lượng của tế bào, mô và dịch sinh học. Khi được tích hợp với dữ liệu omics bổ sung khác, phân tích proteomics có thể cung cấp những hiểu biết mới về cơ chế phân tử của bệnh và xác định các dấu ấn sinh học mới để chẩn đoán và/hoặc tiên lượng và đề xuất các mục tiêu điều trị để điều trị tốt hơn. Phân tích proteomics dựa trên MS gần đây đã được áp dụng cho các EV có nguồn gốc từ tế bào ung thư, tiết lộ các con đường sinh tổng hợp quan trọng và cải thiện sự hiểu biết của chúng ta về quá trình gây ung thư và tiến triển của khối u5. Hàng nghìn đến hàng chục nghìn protein đã được báo cáo trong nhiều nghiên cứu về exosome proteomics được đăng trên các tuyển tập cộng đồng như ExoCarta6 và Vesiclepedia7, 8
Thách thức của Exosome trong điều trị ung thư
Exosome có những lợi thế lớn trong điều trị ung thư, chủ yếu là vì chúng có thể tăng khả năng nhắm mục tiêu phân phối thuốc và có hiệu quả phân phối cao hơn. Tuy nhiên, vẫn còn nhiều thách thức để chuẩn bị các mẫu exosome có độ tinh khiết cao mà không bị nhiễm các protein khác từ dịch sinh học hoặc các vi nang khác. Vì các vi nang được tạo ra bởi một cơ chế tế bào riêng biệt và có chức năng và hàng hóa riêng biệt so với exosome, nên việc tách hai thành phần này trong quá trình phân tích proteomic là điều cần thiết. Do đó, việc thiết lập công nghệ phân lập exosome chuẩn và nhanh hiện đang phải đối mặt trong lĩnh vực thách thức điều trị ung thư. Đồng thời, mặc dù exosome có ý nghĩa sinh học và chuyển dịch quan trọng, nhưng vẫn còn thiếu các dấu ấn sinh học protein phổ quát thực sự có thể xác định phân nhóm EV này. Do đó nên chú ý đến nguồn gốc tế bào trong điều trị ung thư, để tránh ảnh hưởng đến đặc điểm phân phối của exosome khối u có thể thúc đẩy tiến triển ung thư. Vì lý do này, việc mô tả chính xác đặc điểm của exosome cũng là một thách thức trong lĩnh vực điều trị ung thư. Những thách thức bổ sung đối với các nghiên cứu dựa trên MS về exosome bao gồm mức vật liệu bắt đầu thấp và các mức độ pha loãng khác nhau.
Việc xác định các dấu ấn sinh học phổ quát được biểu hiện phong phú của exosome có thể có ý nghĩa tức thời và sâu rộng, cho phép cộng đồng nghiên cứu phát triển các kỹ thuật dựa trên sinh hóa hiệu quả và cụ thể hơn để xác định, mô tả và tinh chế exosome. Hơn nữa, nghiên cứu chức năng của các protein hiện diện phổ biến có thể dẫn đến những hiểu biết mới về các cơ chế cơ bản chi phối sinh học exosome, chẳng hạn như sinh tổng hợp, khả dụng sinh học trong lưu thông và vận chuyển tế bào.
Tài liệu tham khảo:
1. H. Kalra, G. P. Drummen, and S. Mathivanan. Focus on Extracellular Vesicles: Introducing the Next Small Big Thing, Int J Mol Sci 2016, 17(2), 170.
2. G. van Niel, G. D’Angelo, and G. Raposo. Shedding light on the cell biology of extracellular vesicles, Nat Rev Mol Cell Biol 2018, 19(4), 213-228.
3. A. Hoshino, B. Costa-Silva, T. L. Shen, G. Rodrigues, A. Hashimoto, M. Tesic Mark, H. Molina, S. Kohsaka, A. Di Giannatale, S. Ceder, S. Singh, C. Williams, N. Soplop, K. Uryu, L. Pharmer, T. King, L. Bojmar, A. E. Davies, Y. Ararso, T. Zhang, H. Zhang, J. Hernandez, J. M. Weiss, V. D. Dumont-Cole, K. Kramer, L. H. Wexler, A. Narendran, G. K. Schwartz, J. H. Healey, P. Sandstrom, K. J. Labori, E. H. Kure, P. M. Grandgenett, M. A. Hollingsworth, M. de Sousa, S. Kaur, M. Jain, K. Mallya, S. K. Batra, W. R. Jarnagin, M. S. Brady, O. Fodstad, V. Muller, K. Pantel, A. J. Minn, M. J. Bissell, B. A. Garcia, Y. Kang, V. K. Rajasekhar, C. M. Ghajar, I. Matei, H. Peinado, J. Bromberg, and D. Lyden. Tumour exosome integrins determine organotropic metastasis, Nature 2015, 527(7578), 329-35.
4. H. Peinado, H. Zhang, I. R. Matei, B. Costa-Silva, A. Hoshino, G. Rodrigues, B. Psaila, R. N. Kaplan, J. F. Bromberg, Y. Kang, M. J. Bissell, T. R. Cox, A. J. Giaccia, J. T. Erler, S. Hiratsuka, C. M. Ghajar, and D. Lyden. Pre-metastatic niches: organ-specific homes for metastases, Nat Rev Cancer 2017, 17(5), 302-317.
5. M. Nawaz, G. Camussi, H. Valadi, I. Nazarenko, K. Ekstrom, X. Wang, S. Principe, N. Shah, N. M. Ashraf, F. Fatima, L. Neder, and T. Kislinger. The emerging role of extracellular vesicles as biomarkers for urogenital cancers, Nat Rev Urol 2014, 11(12), 688-701.
6. S. Keerthikumar, D. Chisanga, D. Ariyaratne, H. Al Saffar, S. Anand, K. Zhao, M. Samuel, M. Pathan, M. Jois, N. Chilamkurti, L. Gangoda, and S. Mathivanan. ExoCarta: A Web-Based Compendium of Exosomal Cargo, J Mol Biol 2016, 428(4), 688-692.
7. H. Kalra, R. J. Simpson, H. Ji, E. Aikawa, P. Altevogt, P. Askenase, V. C. Bond, F. E. Borras, X. Breakefield, V. Budnik, E. Buzas, G. Camussi, A. Clayton, E. Cocucci, J. M. Falcon-Perez, S. Gabrielsson, Y. S. Gho, D. Gupta, H. C. Harsha, A. Hendrix, A. F. Hill, J. M. Inal, G. Jenster, E. M. Kramer-Albers, S. K. Lim, A. Llorente, J. Lotvall, A. Marcilla, L. Mincheva-Nilsson, I. Nazarenko, R. Nieuwland, E. N. Nolte-‘t Hoen, A. Pandey, T. Patel, M. G. Piper, S. Pluchino, T. S. Prasad, L. Rajendran, G. Raposo, M. Record, G. E. Reid, F. Sanchez-Madrid, R. M. Schiffelers, P. Siljander, A. Stensballe, W. Stoorvogel, D. Taylor, C. Thery, H. Valadi, B. W. van Balkom, J. Vazquez, M. Vidal, M. H. Wauben, M. Yanez-Mo, M. Zoeller, and S. Mathivanan. Vesiclepedia: a compendium for extracellular vesicles with continuous community annotation, PLoS Biol 2012, 10(12), e1001450.
8. M. Pathan, P. Fonseka, S. V. Chitti, T. Kang, R. Sanwlani, J. Van Deun, A. Hendrix, and S. Mathivanan. Vesiclepedia 2019: a compendium of RNA, proteins, lipids and metabolites in extracellular vesicles, Nucleic Acids Res 2019, 47(D1), D516-D519.